2. Morphologie et plan d'organisation
Les insectes représentent un groupe extrêmement varié, et cela, en termes de taille, de morphologie, de couleur, d’écologie ou de comportement. En ce qui concerne la taille, les insectes sont généralement de petite taille, ainsi la taille moyenne des espèces oscille entre un et dix millimètres, cependant, il existe des extrêmes allant de l’insecte microscopique à l’insecte géant, les Mymaridae sont, par exemple, de minuscules Hyménoptères parasites avec un record pour Megaphragma mymaripenne dont la taille ne dépasse pas les 200 µm ce qui rend l’animal plus petit qu’une paramécie [Alexey, 2011]. À l’inverse, certaines espèces de Lepidoptères – comme Troides alexandrae - ou de Phasmes – comme Phobaeticus chani - peuvent atteindre plus de trente centimètres. À savoir qu’à l’époque du Carbonifère supérieur, les insectes avaient des tailles bien supérieures, certaines libellules primitives atteignaient, en effet, plus de soixante-dix centimètres d’envergure.

Figure 3 : Taille de Megaphragma mymaripenne (A) comparée à celle de deux protozoaires, Paramecium caudatum (B) et Amoeba proteus (C), le trait représente 200 µm © Polilov
Les plus petits insectes sont plus petits que les plus grands Protozoaires et les plus grands dépassent les plus petits mammifères – Folsom.
Malgré d’énormes différences entre les ordres, les familles voire les espèces. Les insectes ont tout de même un plan d’organisation commun.
2.1. La paroi du corps
2.1.1. L'épithélium
L’épithélium qu’on appelle aussi épiderme ou encore hypoderme selon l’ouvrage est constitué d’une seule couche de cellules cubiques (épithélium cubique unistratifié), il repose sur une lame basale percée de pores permettant le passage de plus grosses protéines venant de l’hémolymphe [Beaumont, 2000]. La lame basale étant un assemblage de protéines et de glycoprotéines (protéines associées à des sucres) extracellulaires, qui forme une séparation avec l’hémocoele sous-jacent [Beaumont, 2000].
Les cellules épithéliales sont les plus nombreuses (une description de ces cellules est fournie en annexe), elles portent des microvillosités qui sont réduites et tronquées, elles portent aussi des plaques formant des épaississements du cytoplasme où a lieu la dernière étape de la synthèse de la chitine [Beaumont, 2000]. Au niveau apical de ces cellules, il y a des canaux qui vont se ramifier en canaux ciriers (sécrétant de la cire) certains canaux vont arriver jusqu’au coté apical de l’épicuticule et déverser leurs substances [Beaumont, 2000]. La présence de ces canalicules confère à la cuticule un aspect strié.
Dans l’épiderme se trouve un deuxième type de cellules, les glandes épidermiques, prolongées aussi par un canal qui se finit au-dessus de la cuticule.
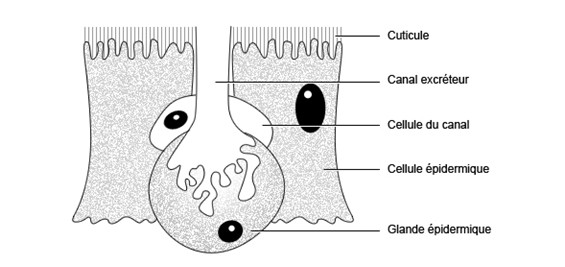
Figure 4 : Dessin d'une cellule glandulaire épidermique © entomoLOGIC (d'après Beaumont modifié)
Il y a un autre type de cellules, les oenocytes. Elles fabriquent une substance cireuse qu’elles transfèrent aux cellules épidermiques, ces cellules se trouvent entre l’épiderme et le tissu adipeux sous-jacent, elles participent notamment à la détoxification cellulaire [Martins, 2012].
Chez la Drosophile, Drosophila melanogaster, les scientifiques sont parvenus à féminiser génétiquement ces oenocytes . Les cires sécrétées contiennent des hydrocarbures, qui servent notamment à la reconnaissance sexuelle chez les insectes (phéromones). Cette modification a rendu des mâles génétiquement modifiés attractifs pour d’autres mâles [Wicker-Thomas, 2009].
L’épiderme participe également à la confection de soies ou d’épines présentes chez beaucoup d’Arthropodes (phasme à tiares, pinces de langoustine, etc.) ou encore d’écailles comme sur les ailes des Papillons. La couleur de ces animaux peut être due à plusieurs choses :
- Des pigments qui sont stockés dans l’épiderme (soit dans ou sur les cellules épidermiques, soit dans des cellules ramifiées remplies de pigments appelés les chromatophores ) ou dans les différentes couches de la cuticule.
- La structure physique de la cuticule, la manière dont la cuticule est agencée va faire que la lumière passera plus ou moins bien, la structure absorbant plus ou moins de couleur et nous renverra la couleur de l’animal. Les écailles des ailes des Papillonsdu genre Morpho d’une couleur bleue par exemple.
- Une combinaison entre les deux.

2.1.2. La cuticule
L’épiderme fabrique une substance, la cuticule, répartie en 2 couches, l’épicuticule et la procuticule [Beaumont, 2000].
L’épicuticule se trouve à la surface de la cuticule, elle est en contact avec le milieu extérieur et mesure entre 2 à 3 µm. L’épicuticule est une couche imperméable constituée d’une juxtaposition de 3 sous-couches, la couche de cément, la couche cireuse et l’épicuticule au sens strict.
La couche de cément est constituée de lipoprotéines tannées qui sont produites par des glandes épidermiques dont le canal excréteur traverse toute l’épaisseur de la cuticule. Cette couche à une épaisseur d’1 µm et peut être absente.
La couche cireuse, appelée également, couche moyenne de cire est composée de paraffine, d’acide gras et d’alcools à longues chaines, cette couche mesure de 0,5 à 1 µm d’épaisseur et permet de limiter les pertes en eau. La cire est produite par les oenocytes et emprunte les canaux poraires (ou canalicules des pores). Ces canaux sont des digitations des cellules épidermiques qui traversent toute l’épaisseur de la procuticule, à partir du moment où ils passent dans l’épicuticule les canaux poraires prennent le nom de canaux ciriers.
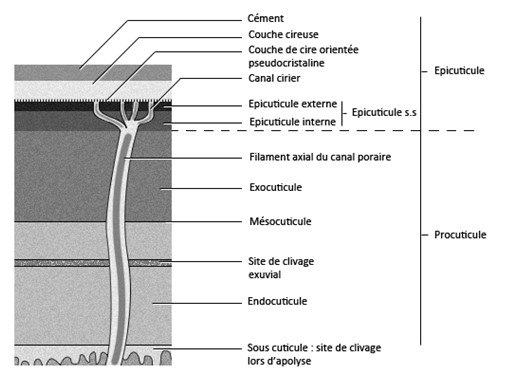
Figure 6 : Structure de la cuticule © entomoLOGIC
La couche cireuse et la couche de cément sont qualifiées de couches postexuviales, elles ne seront sécrétées que quand l’animal changera de cuticule. Par opposition à la dernière couche, l’épicuticule au sens strict.
L’épicuticule au sens strict fait 0,5 µm d’épaisseur et sert à la fois, à la fixation des muscles ainsi qu’à la transmission des signaux chimiques (aussi appelés phéromones). Cette couche est faite de lipoprotéines tannées et en particulier, la cuticuline, il s’agit d’une couche prééxuviale subdivisée en deux parties, L’épicuticule externe ou cuticuline et l’épicuticule interne.
L’épicuticule externe mesure 20 nm d’épaisseur. En période d’intermue elle a une structure trilaminaire. L’épicuticule interne, quant à elle, mesure de 0,2 à 0,5 µm d’épaisseur. Cette sous couche est riche en protéines, en composés aromatiques et contient des stérols.
Les deux autres couches, l’exocuticule et l’endocuticule, forment la procuticule. Elles contiennent de la chitine, qui est une substance synthétisée à partir du tréhalose (dimère de glucose regroupé par des liaisons α, α. 1-1). La chitine est un dimère de glucosamine qui polymérise en filament dans l’hémolymphe, sur ce filament vont se greffer des protéines ou d’autres molécules. Cette molécule a un rôle protecteur, car lorsqu’elle est associée à du carbonate de calcium, elle devient très rigide et forme l’exosquelette des Crustacés et la coquille d’autres animaux. Cependant ce n'est pas la chitine qui est le principal élément rigide de la cuticule, mais une protéine très particulière appelée la sclérotine qui la compose à 80%.
L’exocuticule est sécrétée avant la mue, il s’agit donc d’une couche pré-éxuviale, qui est dure et colorée, elle présente, en effet, des stratifications de couleur ambrée. La chitine est associée à des protéines tannées (la sclérotine), cette protéine rend la couche rigide colorée.La mélanine y est également présente pour donner la coloration brunâtre-noirâtre propre à beaucoup d’insectes. Cette couche représente d’un douzième à la moitié de l’épaisseur totale de la cuticule.
L’endocuticule est une couche contenant encore plus de chitine, ce qui la rend plus souple. De plus elle est associée à l’arthropodine qui est également une protéine souple.
L’exocuticule et l’endocuticule peuvent être séparées par une mésocuticule.
La procuticule est fréquemment séparée de l’épiderme par une couche assez anarchique composée de mucopolysaccharides acides, la sous-cuticule. Le rôle de cette sous-cuticule n’est pas encore
connu, bien qu’une hypothèse décrit cette couche comme étant un « lubrifiant » qui servirait aussi à l’osmorégulation des différents milieux. (L’osmorégulation consiste à l’équilibre
ionique entre les différents milieux).
2.1.3. Composition chimique
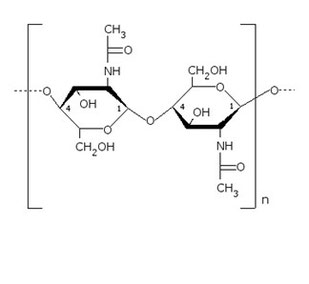
LA CHITINE
La chitine est un polysaccharide azoté et acétylé qui représente environ 50% du poids sec de la cuticule des Insectes, c’est un composé qui se polymérise très facilement et qui porte le nom de poly-acétyl-D-glucosamine. Chimiquement il s’agit d’un C8H13O5N répété n fois. L’hydrolyse de ce composé fournit de la glucosamine [Wikipedia, 2014].
Tout d’abord une fonction acétyle s’associe au niveau de l’azote porté par le carbone 2 de la glucosamine, cette association fournit de l’acétyl-glucosamine, il s’agit de l’élément unitaire conduisant à la fabrication de la chitine. Dans un second temps, deux de ces molécules s’assemblent par une liaison osidique pour former du tréhalose, ou chitobiose [Wikipedia, 2014].
Au niveau de l’hémolymphe, la chitine se polymérise, les polymères s’assemblent parallèlement entre eux par des ponts latéraux en formant des micelles allongées à disposition pseudo-cristalline.
La chitine est une substance souple et perméable à l’eau du fait de sa nature sucrée. Il n’existe donc aucun rapport entre la richesse en chitine et la dureté du tégument. La disposition de la chitine fait qu’elle s’assemble à d’autres molécules, ce sont ces molécules qui seront responsables de la dureté du tégument des Insectes [Beaumont, 2000].
LES PROTEINES TANNEES
Elles représentent 25 à 75% du poids sec de la cuticule. Elles peuvent être révélées par les techniques de révélations de protéines comme le Western Blot. Afin de s’insérer dans la chitine qui est une molécule hydrophile, les protéines doivent présenter une portion hydrophile, comme l’arthropodine, et une portion hydrophobe, comme la sclérotine responsable de la dureté des téguments [Beaumont, 2000].
Arthropodine et sclérotine ne représentent pas des protéines particulières, mais des groupes de protéines caractérisés par leurs propriétés assez identiques (poids moléculaire, charge des molécules qui provoque une mobilité plus ou moins importante en électrophorèse, solubilité, etc.) d’association à la chitine [Beaumont, 2000].
En réalité arthropodines et sclérotines ne se différencient que par leur état physique, d’ailleurs leur séquençage en acides aminés ne révèle aucune différence. Les sclérotines sont des protéines cuticulaires banales, elles sont stabilisées par un tannage quinonique agissant sur les NH2 libres des protéines dans l’exocuticule, ceci n’affecte pas les arthropodines, mais rend l’exocuticule plus dure [Beaumont, 2000].
LES CUTICULINES
L’épicuticule est dépourvue de chitine, elle contient par contre de nombreuses substances assez mal connues. La cuticuline présente dans l’assise profonde résiste à l’action des solvants organiques et aux acides minéraux. C’est une lipoprotéine tannée par des quinones [Beaumont, 2000].
La couche cireuse est riche en un mélange de paraffines en C27 et C31, d’esters d’alcool supérieurs et d’acides gras non saturés en C26 et C30. Les chaines hydrophobes sont orientées perpendiculairement à la surface. Les pôles hydrophiles sont vers l’intérieur. Les pôles hydrophobes confèrent l’imperméabilité du tégument. Mettre un Insecte dans un détergent provoque sa mort immédiate. Ceci est d’ailleurs utilisé dans de nombreux insecticides [Beaumont, 2000].
2.1.4. Conséquence de la présence de la cuticule
La cuticule forme un véritable exosquelette, de ce fait il faut que l’animal s’adapte morphologiquement et physiologiquement.
Il existe une diversité des formations tégumentaires qui va avec la diversité morphologique des Insectes. Cependant, l’anatomie de ces animaux reste tout de même plus ou moins identique en fonction des ordres .
Il n’existe aucun cil vibratile à la surface de tous les épithéliums ectodermiques, notamment sur l’épiderme. Cependant, des formations ciliaires peuvent tout de même apparaitre de manière transitoire au cours de l’organogenèse des glandes ou des structures sensorielles [Beaumont, 2000].
Les mouvements relatifs des métamères ne sont possibles que grâce aux membranes articulaires où la cuticule est amincie et dépourvue d’exocuticule. L’abdomen des Insectes comporte des déformations très fréquentes dues aux variations volumétriques (alimentations et maturation des œufs chez les femelles). Les pleurites non sclérotinisées constituent, avec les membranes articulaires adjacentes, des zones souples et extensibles [Morin, 2014].
Pour une articulation, tous les mouvements ne sont pas possibles, en effet les articulations mettent en jeu 2 condyles au maximum, ce sont des articulations monocondylaires et des articulations dicondylaires. Ces articulations sont disposées selon deux modalités [Beaumont, 2000]. Les articulations intrinsèques où le condyle et la cavité glénoïde sont différenciés au sein de la membrane articulaire et les articulations extrinsèques, où les formations complémentaires se situent à l’extérieur des membranes articulaires [Beaumont, 2000].
Même si les articulations ne favorisent qu’au maximum deux plans de l’espace, la combinaison de ces articulations fait que les Arthropodes peuvent réaliser des mouvements complexes dans tous les plans de l’espace (mouvements omnidirectionnels).
Les muscles ont une action puissante, la cuticule à elle seule ne pourrait pas supporter les contractions, c’est pourquoi les faisceaux musculaires s’insèrent au niveau d’invaginations tégumentaires qu’on nomme apodèmes [Roth, 1974]. L’ancrage des fibres musculaires se fait par des invaginations de la membrane plasmique et sarcoplasmique, de plus de multiples desmosomes et microtubules forment un cytosquelette permettant la cohésion de l’ensemble. À chaque mue, cette association doit être renouvelée [Beaumont, 2000].

2.1.5. Mue et déroulement de la mue
La présence d’un exosquelette rigide et par définition inextensible confère à la croissance des Insectesun caractère discontinu.
À la sortie de l’œuf, l’animal se développe, seulement il ne pourra le faire qu’en changeant sa cuticule et en grandissant pendant ce changement de cuticule
Il arrive un moment où la cuticule devient trop petite pour la croissance ou pour les changements, l’animal va donc muer, la mue est un phénomène permettant la croissance discontinue de l’animal, elle se fait en plusieurs étapes [Beaumont, 2000].
Tout d’abord, il y a activation des cellules épidermiques, elles entrent en mitose, ceci est suivi d’un autre phénomène, l’apolyse. À ce moment, la cuticule commence à se décrocher, ceci se fait plusieurs jours avant la mue.
L’endocuticule, ayant été dégradée, va prendre l’aspect d’un liquide, le liquide exuvial. Ce liquide sera réabsorbé en grande partie par l’épiderme. Entre temps, les oenocytes commencent à sécréter de la cire qui sera transmise aux cellules épithéliales, il y aura formation de canalicules des pores et dépôt de cires sur la nouvelle cuticule.
Le gel continuant à agir, Il y a des endroits où la cuticule devient très fine, ces endroits sont appelés lignes d’exuviation, l’animal va se gonfler d’eau ou d’air et va casser la cuticule au niveau ces lignes, il y a alors exuviation.
L’exuviation, encore appelée ecdysis va permettre à l’animal de sortir de son ancienne cuticule. Pendant ce temps, les cellules épidermiques ont proliféré, provoquant ainsi un plissement de l’épiderme, après l’exuviation l’épiderme va se déplier et l’animal va grandir, laissant derrière lui son ancien exosquelette encore nommé exuvie.
Le reste de la cuticule est alors synthétisé, il y a tannage des protéines et sclérotinisation. Les couches post ecdysiales sont ensuite synthétisées. Pendant cette période l’animal reste à jeun,
en effet il ne se nourrit qu’après que ça cuticule soit reformée, ce qui explique que la croissance en terme de poids a une allure assez différente à la croissance en longueur.
Le rapport des tailles successives prises par les Insectes au cours de leur développement post embryonnaire a en général une valeur constante de 1,25. La longueur augmente donc du quart à chaque mue, c’est la règle de Prizbram. Le poids, quant à lui, double d’une mue à l’autre, c’est la règle de Dyar.
L’activation de la mue est sous le contrôle d’une hormone stéroïde, l’ecdysone. Cette hormone est sécrétée par la glande de mue aussi appelée glande prothoracique chez les insectes [Beaulaton, 1968]. Plus précisément, à la suite de sa sécrétion, l’hormone est activée par d’autres organes et va contrôlée la phase pré-éxuviale de la mue.
Chez les insectes, les mues de métamorphoses se produisent quand l’ecdysone est sécrétée en absence d’une autre hormone, l’hormone juvénile (contrôlant le développement post-embryonnaire), elle-même sécrétée par les corps allates [Lauga-Reyrel, 1984]. À l’inverse, les mues juvéniles sont déclenchées après sécrétion d’ecdysone en présence d’hormone juvénile.
2.1.6. Les métamorphoses
Chez les insectes, une métamorphose est une mue qui s’accompagne de changements morphologiques, anatomiques ou physiologiques très importants chez l’animal. Quand elle existe, elle peut se faire en une ou deux étapes. Une première classification peut alors se faire en fonction de ce critère.
LES INSECTES AMETABOLES
Ce sont les insectes qui ne présentent aucune métamorphose. Le type amétabole est généralement considéré comme le type de développement ancestral chez les insectes [Lafont, 2011]. Il n’y a pas de stade larvaire défini, seules la taille et la capacité de se reproduire différencient la juvénile de l’adulte [Larousse, 1971]. On peut trouver ce type de développement chez les Archéognathes et les Zygentomes [Lafont, 2011].

LES INSECTES HETEROMETABOLES
Le développement larvaire amène progressivement à l’adulte, appelé imago. Cependant il n’y a pas de stade nymphal individualisé (stade du développement de certains insectes caractérisés par l’absence de prise alimentaire). Ce sont les insectes à métamorphose incomplète ou progressive. Les larves présentent des caractères adultes qui se développent au fur et à mesure de chaque mue larvaire, c’est le cas des fourreaux alaires (ou ptérothèques) par exemple [Larousse, 1971].
Ce schéma peut, cependant, varier. Ainsi, si les larves sont aquatiques et les adultes aériens ou terrestres, leur développement sera qualifié d’hémimétabole. C’est le cas des Odonates ou des Perles [Larousse, 1971].

A l’inverse, si les larves ne présentent pas d’adaptations à la vie aquatique. Le développement sera qualifié de paurométabole [Larousse, 1971].

Le développement des caractères adultes peut être plus ou moins tardif. Dans le cas où le développement des ailes n’est pas visible pendant la phase larvaire, le développement est qualifié de néométabole. Ce type de développement est visible chez les Thysanoptères [Larousse, 1971].
Toujours dans cet ordre d’insecte, les deux derniers stades larvaires se déroulent dans des conditions qui rappellent les vraies nymphes des holométaboles. L’animal ne se nourrit pas et est très peu actif, la mue s’accompagne de changements dans les pièces buccales et les antennes qui s’atrophient. Larve et adultes sont cependant très proches morphologiquement parlant. Le développement est ici qualifié de remétabole [Larousse, 1971].

De la même façon, chez les Chermesidae (Hémiptère) et les Phylloxeridae (Hémiptère), les ébauches alaires n’apparaissent qu’au dernier stade larvaire et se développent très rapidement. Ce stade, abusivement nommé nymphe est typique de ces groupes, c’est pourquoi leur type de développement particulier est qualifié d’homométaboles [Dajoz, 2010].
Chez les larves femelles de Cochenilles, le développement est de type paurométabole, cependant chez les mâles le développement larvaire nécessite deux mues supplémentaires qui vont donner à la larve un aspect et un comportement de nymphe ayant des ébauches alaires. Ce type de développement particulier est qualifié de paramétabole [Dajoz, 2010].
Chez les Aleurodidae (Hémiptère), les larves diffèrent des imagos par un ensemble de caractères morphologiques, la dernière mue libère un imago normal aux ailes et aux pattes développées. Ce dernier stade larvaire n’est cependant pas une nymphe, bien qu’elle s’en rapproche beaucoup. Ce type de développement est qualifié d’allométabole [Dajoz, 2010].
Enfin, chez les éphémères, le développement est de type hémimétabole, cependant un stade subimago s’intercale entre le dernier stade larvaire aquatique et l’adulte aérien. Ce type de
développement est unique chez les insectes, mais ne porte pas de nom particulier [Larousse, 1971].
La durée du stade subimago est très variable, à peine sortie de son ancienne enveloppe le subimago s’envole rapidement vers la végétation riveraine et attendra quelques minutes voire quelques jours avant d’effectuer sa dernière mue, les Caenidae présentent la particularité d’effectuer cette mue en plein vol quelques minutes après la dernière exuviation [Les-Moucheurs-Nantais, 2012].

LES INSECTES HOLOMETABOLES
Les larves différent considérablement des adultes. Elles n’ont jamais d’ébauches alaires, elles sont aveugles ou possède des yeux simples. Les antennes et les pattes sont courtes ou inexistantes Généralement, leur habitat et leur biologie n’ont aucun rapport avec ceux des adultes [Larousse, 1971].
Le développement holométabole est caractérisés par un stade d’immobilité, la nymphose, intercalé entre le stade larvaire et l’imago. Ce stade appelé nymphe est délimité par deux mue, la mue nymphale et la mue imaginale.
Durant cette nymphose, il y a une élimination des organes larvaires (muscles, glandes séricigènes, tubes de Malpighi) et une édification des organes adultes. Les organes restants vont cependant subir un remaniement important.
Les organes adultes dérivent, quant à eux, de groupes de cellules, les disques imaginaux, isolés dés le début du développement mais dans un état de repose durant la vie larvaire.

Comme c’est le cas chez les hétérométaboles, il y a des particularités chez certains taxons. C’est le cas des hypermétamorphoses, plusieurs formes larvaires se succèdent avant la nymphose. Ce phénomène est connu chez divers Hyménoptères parasites, les Strepsiptères ou les Meloidae (Coléoptères). Le Chalcidien Stibula éclot sous la forme d’une larve « planidium » agile et poursuit son développement dans une nymphe de fourmi à l’état de larve secondaire ; les Méloés, les Cantharides et autres « vésicants » vivent aux dépens d’Abeilles ou de Criquets et montrent successivement une larve primaire (triongulin), deux larves secondaires, une pseudonymphe et une larve tertiaire avant de se nymphoser. Toutefois, le passage d’une forme larvaire à l’autre se réalise sans remaniement tissulaire ; celui-ci ne s’accomplit que chez la nymphe proprement dite [Larousse, 1971].

Enfin, les stades le stade larvaire peut disparaitre. Le développement peut être qualifié de cryptométabole [Naturimages, 2014].
2.1.7. Les membranes articulaires
Les membranes articulaires se trouvent entre les différents métamères, au niveau des soies et au niveau des pattes, la membrane articulaire possède une protéine particulière appelée la résine. De plus, elle ne possède pas d’exocuticule.
2.1.8. Les soies
La cuticule peut, chez certains insectes, être ornée de baguettes chitineuses, les soies, il y en a deux types :
- Les soies pleines qui sont, en général, ornementales, cette soie est sécrétée par une cellule trichogène, cette cellule est entourée par une autre cellule qui la protège, la cellule tormogène.
Les soies sont aplaties chez les Lépidoptères et ont un aspect écailleux. Chez l’abeille les soies au niveau des pattes ont un rôle protecteur mais servent aussi à récolter le pollen [Beaumont, 2000].
- Les soies sensorielles qui ont la même organisation que les soies pleines mais qui sont reliées à une cellule nerveuse avec des dendrites qui sont dans la soie. La cellule nerveuse est entourée dans une cellule téchogène, le tout est entouré par la cellule trichogène puis par la cellule tormogène [Beaumont, 2000]. Une soie ayant une cellule nerveuse portant plusieurs dendrites est appelée sensille. Les soies sensorielles peuvent être de deux types, gustatives et olfactives.
- Les soies gustatives se trouvent souvent sur les pièces buccales et se terminent par un pore gustatif (non représenté sur le schéma) permettant à l’animal de gouter.
- Les soies olfactives s’ouvrent quant à elles par plusieurs pores (non représentés sur le schéma) qui permettent de capter une information olfactive, elles se trouvent au niveau des antennes.
2.2. Réalisation de la métamérie
Le corps des Insectes est constitué d’éléments semblables qu’on nomme métamères, ceux-ci sont reliés les uns aux autres par de souples membranes. Ces métamères se forment au cours du développement embryonnaire de l’animal [Salgueiro, 2002].
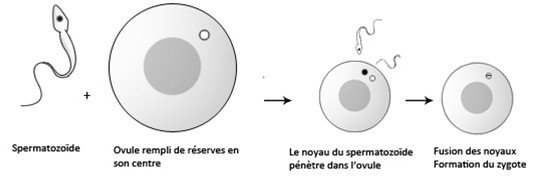
Lors de la fécondation, le spermatozoïde et l’ovule fusionnent conduisant à la formation d’une cellule œuf qu’on nomme le zygote, cette cellule se divise plusieurs fois pour devenir un embryon. Cet amas de cellules appelé blastula entoure une cavité qu’on nomme le blastocœle.

Pendant la gastrulation, les cellules de la blastula migrent dans le blastocœle de façon à s’organiser en 3 feuillets embryonnaires, l’ectoderme à l’extérieur, l’endoderme à l’intérieur et le mésoderme entre les deux autres feuillets.
Le mésoderme se creuse d’une cavité, qu’on nomme le cœlome, celui-ci se scinde en plusieurs petites cavités.
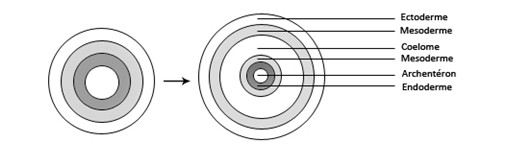
Les métamères correspondent à la répétition tout le long du corps (de la tête à l’anus) de la même organisation cellulaire autour d’une paire de cavités cœlomiques.
Une fois les métamères formés, les parois des vésicules cœlomiques métamérisées vont se dissocier très rapidement. Ces vésicules vont alors fusionner avec le blastocoele embryonnaire, une nouvelle cavité va donc se former, l’hémocoele, dans cet hémocoele circule un liquide qu’on nomme hémolymphe. Chez l’adulte il n’y aura plus grand-chose qui sera originaire du cœlome embryonnaire, le cœlome est en effet vestigial, il formera la cavité des glandes génitales avec une portion initiale, ou saccule, de certains organes excréteurs segmentaires.
En se dégradant, les parois des vésicules cœlomiques vont devenir des muscles, ces muscles ont une organisation particulière chez les Insectes. En effet il n’y a plus de muscles circulaires, les Insectes ne se déplacent plus par les mouvements du corps, mais par les mouvements de leurs pattes articulées.
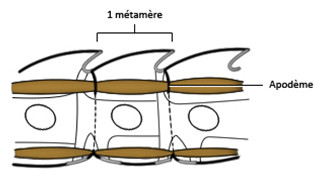
Du fait de cette fusion des vésicules cœlomiques avec le blastocœle, la métamérie chez les Insectes est difficile a observer à l’intérieur du corps, cependant elle reste plus ou moins visible à l’extérieur, puisqu’elle est encore altérée par la tagmatisation du corps.
Le corps des Insectes résulte donc de la juxtaposition longitudinale de métamères. La disposition régulière de ces unités structurales et fonctionnelles se traduit par une répartition périodique des organes ou fragments d’organes. Chaque métamère est encadré par plusieurs plaques squelettiques, une pièce dorsale, le tergite, une pièce ventrale, le sternite et deux pièces latérales souvent fusionnées, les pleurites qui sont dorsales et les épimérites qui sont ventrales.
Ces différentes pièces sont réunies par des zones articulaires souples et minces qui sont également présentes entre les métamères. Le métamère est traversé par la chaine nerveuse ventrale, le tube digestif et le vaisseau dorsal. Il renferme une paire de ganglions, deux faisceaux musculaires dorsaux et deux faisceaux musculaires ventraux. Ces muscles sont insérés sur des replis de la cuticule, les apodèmes. Ces apodèmes marquent les limites antérieures et postérieures des métamères.
Chaque métamère porte deux appendices composés de plusieurs articles, ces appendices sont insérés entre les pleurites et les épimérites. Chaque métamère est donc un ensemble complexe comprenant un segment ectodermique limité par des sillons intersegmentaires, un segment vasculaire composé du vaisseau dorsal, un segment digestif, un segment nerveux appelé également neuromère, un segment musculaire composé des muscles ventraux et dorsaux ainsi que des muscles des pattes appelé aussi le myomère, un segment excréteur aussi appelé néphromère et une paire d’appendices appelée également segment appendiculaire [Beaumont, 2000].
Tous ces éléments résultent d’une intégration anatomique et physiologique au sein du métamère. Tous les composants sont liés les uns aux autres.
Chez les Insectes, on distingue l’acron, le tronc ou soma composé de la juxtaposition des métamères vrais et le telson. L’acron et le telson ne sont pas des métamères. L’acron n’est pas forcément visible, il renferme le cerveau primitif, qui est dorsal, le protocerebron encore appelé archicérébron. Il ne s’agit pas d’un métamère car il ne contient pas de sac cœlomique. La bouche s’ouvre en arrière de l’acron, au niveau du premier métamère vrai. Le telson est toujours bien visible, il est dépourvu de ganglions nerveux et de vésicules cœlomiques, il porte l’anus.
2.3. La tagmatisation
Contrairement aux Annélides (vers annelés), les divers métamères des Insectes sont dissemblables, on parle de métamérie hétéronome. Ils s’ordonnent de manière à former des régions morphologiquement distinctes. Cette spécialisation est accompagnée de la fusion des métamères dont les appendices collaborent à la réalisation de la même fonction (locomotion, mastication, reproduction, perception sensorielle) [Roth, 1980].
Les métamères et les appendices associés qui constituent le soma vont fusionner pour former des tagmes, ces tagmes vont être morphologiquement différents et vont être spécialisés dans des fonctions [Roth, 1980].
La tête est la zone des sens, il s’agit d’un tagme assez homogène où ne sont plus distinguables les segments originels. Elle sert à la perception sensorielle et à la prise alimentaire.
Le thorax sert à la locomotion, il est séparé en 3 parties, le prothorax, le mésothorax et le métathorax. Chaque segment porte une paire de pattes qui servent à se déplacer, les deux derniers peuvent aussi porter une paire d’ailes et forment le ptérothorax des Ptérygotes. Récemment, une étude a été menée sur la famille des Membracidae (Hémiptères) et a montré que leur prothorax portait une paire d’ailes surnuméraire qui aurait dérivé leur « casque » [Prud'homme, 2011]. Ceci n’est pas très étonnant puisque les premiers Ephéméroptères possédaient 3 paires d’ailes [David, 2005].
L’abdomen sert à la reproduction. A l’origine, il comprend une douzaine de segments, cependant, après fusions il en comportera moins.
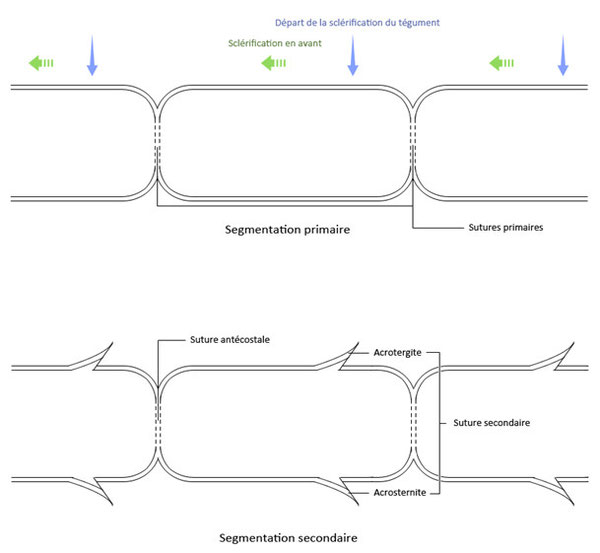
Cette segmentation paraissant ainsi simpliste est en réalité beaucoup plus complexe, en effet, le corps de l’insecte, du moins sa segmentation apparente, est le résultat d’une métamérisation secondaire qui a lieu lors de la sclérification du tégument. En effet la sclérification d’un segment ne se fait qu’à à sa partie antérieure, elle atteint ensuite la suture primaire puis la partie postérieure du segment précédent, il y a un décalage antérieur qui créé une deuxième ligne de sutures [Roth, 1980].
La suture primaire, trace de la segmentation primaire, portera les muscles et sera appelée suture antécostale. La suture secondaire portera le nom d’acrotergite ou d’acrosternite selon qu’il s’agit d’une suture dorsale ou ventrale [Roth, 1980].
2.3.1. La tête
LA METAMERIE CEPHALIQUE
La tête est une partie assez homogène résultant de la fusion de l’acron et de plusieurs métamères. Le nombre de métamères entrant dans la formation de la tête est discuté selon les auteurs. Pour la plupart d’entre eux, la tête résulterait de la fusion de l’acron encore appelée protocéphalon et de 5 métamères vrais avec leurs appendices associés [Roth, 1980].
- Protocéphalon : Yeux
- Métamère 1 : Antennes
- Métamère 2 : -
- Métamère 3 : Mandibules
- Métamère 4 : Maxilles
- Métamère 5 : Labium
Pour d’autres auteurs, la tête serait constituée de 6 métamères vrais et de l’acron. D’autres auteurs affirment que la tête est composée de plusieurs autres métamères. Handlirsch affirme par exemple qu’il existe un métamère oculaire, car dans son étude, en coupant l’œil d’un crustacé, il a pu remarquer la régénération d’un nouvel appendice [Roth, 1980].
Selon Chaudonneret la tête résulterait de la fusion de seulement 7 métamères
- Métamère 1, métamère préantennulaire ou protocéphalon : yeux et ocelles, aucun appendice. Le neuromère correspondant est le protocérébron.
- Métamère 2 ou métamère antennulaire : antennes. Le neuromère correspondant est le deutocérébron
- Métamère 3 ou métamère antennaire : dépourvu d’appendices, correspond au tricérébron
- Métamère 4 ou métamère superlingual : dépourvu d’appendices chez la plupart des Insectes sauf chez certains où il correspondrait au superlinguae. L’existence de ce métamère est très controversée
- Métamère 5 ou métamère mandibulaire : mandibules
- Métamère 6 ou métamère maxillaire : maxilles
- Métamère 7 ou métamère labial : labium
SUTURES
La tête est constituée de plusieurs pièces séparées par des sutures [Jeannel, 1946 ; Roth, 1980].
- La suture épicrânienne qui n’est pas toujours bien marquée. Elle porte des noms différents en fonction de sa localisation :
- La suture coronale ou métopique : elle divise le dessus de la tête en deux parties. Lorsqu’il y a 3 ocelles, deux se trouvent de part et d’autre de la suture coronale, le médian se trouvant sur la partie supérieure du front. Chez les ptérygotes les plus évolués les sutures frontales sont invisibles à l’œil nu cependant, la suture coronale se scinde en deux branches, les sutures postfrontales, qui passent directement derrière les ocelles, rejoignent les sclérites oculaires puis passent derrière les antennes.
- Les sutures frontales : incomplètes, voire absentes, ce sont deux branches qui font suite à la suture coronale. Elles entourent le front.
- La suture occipitale qui entoure le foramen magnum, elle vient aboutir devant les articulations postérieures des mandibules. Elle porte une crête interne qui renforce la calotte crânienne.
- La suture postoccipitale qui se trouve derrière la suture occipitale, elle porte également des crêtes internes sur lesquelles s’insèrent des muscles prothoraciques d’articulations.
-
Les sutures subgénales qui sont situées des deux côtés de la tête le long de la bouche au-dessus de l’attache des appendices. On les divise en plusieurs
parties
- Les sutures pleurostomales au-dessus des mandibules
- Les sutures hypostomales en arrière
- La suture épistomale à l’avant
Ces sutures forment, intérieurement, une crête soudée aux bras postérieur et antérieurs du tentorium
- Les sutures sous-antennaires qu’on trouve parfois et qui relient le socle des antennes à la suture subgénale
- Les sutures sous-oculaires qui relient, quand on les trouve, les sclérites oculaires et la suture subgénale
- Les sutures oculaires et antennaires qui entourent la base des yeux et des antennes
LES REGIONS CRANIENNES
Les sutures séparent les différentes régions de la tête [Jeannel, 1946 ; Roth, 1980] :
- Le vertex : dessus du crâne pouvant être coupé par la suture coronale
- Le front : région antérieure entourée par les sutures frontales
- Le clypeus : juste sous la région frontale
- Les aires pariétales : les deux parties du vertex séparées par la suture coronale composées :
- des genae : parties des aires pariétale juste sous les yeux, on les nomme aussi les joues.
- des fastigium du vertex : parties hautes des aires pariétales
- des tempes : parties des joues juste derrière les yeux
- Les sclérites antennaires : à la base des antennes et délimités par les sutures antennaires
- Les sclérites oculaires : autour des yeux et délimités par les sutures oculaires
- La région occipitale ou occiput : partie comprise entre les sutures occipitale et postoccipitale
- La région postoccipitale : rebord du foramen magnum
- Les aires subgénales : partie portant les pièces buccales situées sous les sutures pleurostomales
Ces différentes pièces sont modifiées en fonction des ordres d’insectes.






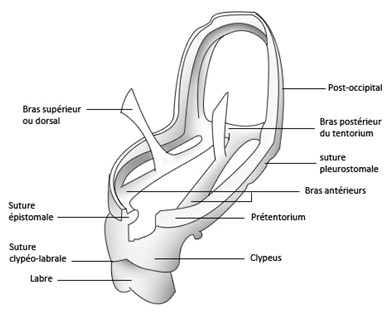
L'ENDOSQUELETTE CEPHALIQUE
En plus des crêtes internes, on trouve une structure particulière qu’on nomme le tentorium, il est constitué par la fusion d’inva-ginations de l’exosquelette qu’on nomme apodèmes. Il intervient dans le soutient des structures internes de la tête, comme les structures nerveuses ou l’intestin antérieure, il renforce également l’exosquelette céphalique en permettant de consolider les points d’articulations des pièces buccales, enfin il sert de zone d’insertion aux principaux muscles céphaliques (Adducteurs des mandibules, adducteurs des maxilles et du labium, rétracteurs de l’hypopharynx et dilatateurs du stomodeum) [Roth, 1980 ; Ramel, 2014].
Le tentorium présente donc plusieurs points d’attaches :
- Les points d’attaches antérieurs se trouvant sur la suture épistomale
- Les points d’attaches postérieurs se trouvant aux extrémités de la suture post occipitale
Ces invaginations cuticulaires se rejoignent pour donner un ensemble de trois bras (2 bras antérieurs reliés à 1 bras postérieur) sur lesquels peuvent s’adjoindre deux bras supérieurs [Ramel, 2014]. Extérieurement, les insertions des bras antérieurs forment les prétentorina, tandis que les insertions postérieures forment les métatentorina.
La forme du tentorium est variable en fonction du type d’insecte, il peut même être inexistant.

MODIFICATIONS POSSIBLES
Les variations sont très nombreuses surtout au niveau de la tête, ceci est principalement dû au régime alimentaire. Ces variations seront donc décrites dans chacun des groupes étudiés.
LES APPENDICES (PIECES BUCCALES, YEUX ET ANTENNES)
Les pièces buccales et les yeux seront étudiés dans une autre partie. Les antennes sont des organes sensoriels qui servent à l’odorat, au toucher ou au goût. Ceci est possible grâce à la présence se sensilles [Jeannel, 1946 ; Roth, 1980].
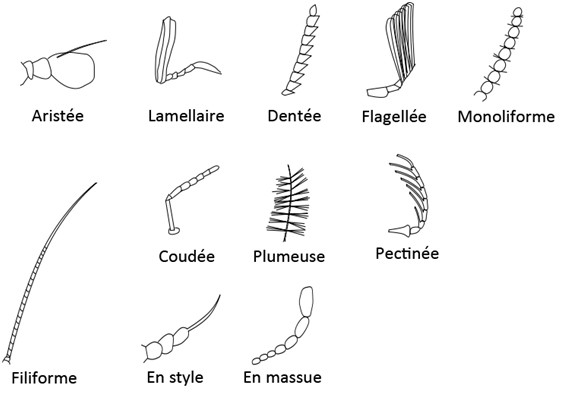
L’antenne est composée de plusieurs segments.
- Le scape : le premier article de l’antenne.
- Le pédicelle : le deuxième article de l’antenne.
- Le flagelle : ensemble des articles a partir du troisième article. Peuvent être distingués :
- Les flagellomères : article du flagelle.
- Les anneli : premiers articles du flagelle.
Même si les articles sont rarement changeants, la forme des antennes est très variable selon l’espèce.
2.3.2. Le thorax
Le thorax est le tagme moteur de l’insecte, il porte dans la plupart des cas 3 paires de pattes locomotrices et 2 paires d’ailes. Des modifications sont également possibles comme la transformation de la paire de pattes prothoraciques des Mantes (Dictyoptera, Mantodea) ou des Mantispes (Neuroptera, Mantispidae) en pattes ravisseuses.
Le thorax est composé de trois métamères, le prothorax, le mésothorax et le métathorax. Tous trois ayant la même structure qu’un métamère classique (notum, sternum et pleures).
Cette partie est très compliquée, puisque la morphologie du thorax dépend de l’ordre voire de la famille. Il ne sera présenté qu’un schéma type.
LE COU
Le cou est aussi nommé servix, c’est une partie négligée dans l’étude des différents tagmes, il n’est pas possible d’en faire un segment à part entière, certains auteurs le nomment, pour cette raison, le microthorax. D’autres auteurs l’attribuent à la partie postérieure du labium. Cependant il est important de noter que des sclérites cervicaux peuvent s’y développer. Son origine est mal connue. À l’heure actuelle, on pense qu’il s’agit d’une structure ayant une double origine (labiale et thoracique) [Roth, 1980].
LE NOTUM
Le notum est la partie dorsale des segments thoraciques. Chez les aptérygotes ou les larves, il ne subit pas de réelles modifications quant à la structure émanant de la métamérisation secondaire (ou tagmatisation). En revanche il est fortement modifié chez les ptérygotes et notamment au niveau du Ptérothorax. Généralement, on observe un développement du mésonotum et du métanotum, qui sont les deux segments portant les ailes, chez les coléoptères c’est le pronotum qui est très développé, de sorte qu’on ne voit même plus les autres segments. Quoi qu’il en soit, le thorax serait, à l’état embryonnaire, composé de 6 métamères, 3 tergites et 3 post-tergites (notum et postnotum) [Roth, 1980].
- Tergite I
- Acrotergite II (ou postnotum I)
- Notum II
- Postnotum II
- Notum III
- Postnotum III
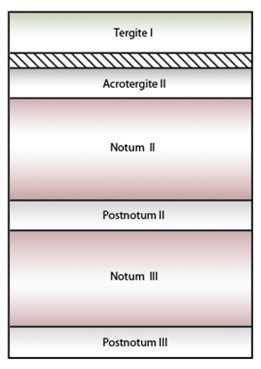
Enfin sur chaque segment il y a des sutures [Roth, 1980] :
- La suture antécostale portant une phragme interne, elle sépare le tergite I de l’acrotergite II.
- La suture scutoscutellaire séparant le notum en deux : le scutum et le scutellum, cette suture est généralement en V retourné, elle porte une crête interne provenant de la déformation du thorax.
- La suture notale qui divise le scutellum en une zone antérieure et deux postérolatérales. Cette suture, en forme de V droit, existe chez les insectes à suture scutoscutellaire évasive, comme les criquets.
- La suture transverse ou préscutale qui sépare le scutum et isole, en avant, le prescutum. On la trouve chez les plécoptères, certains orthoptères, les lépidoptères et les coléoptères.
- Les sutures convergentes (notaulix) qui forment un V droit dans le scutum, chez les hyménoptères.
- La suture notale médiane qui barre le scutum dans le sens de la longueur, chez les hyménoptères.
- La suture transcutellaire, chez les diptères évolués, barrant le scutellum d’un bout à l’autre de la suture scutelloscutellaire.

LE STERNUM
Le sternum est la partie ventrale du thorax, la fusion y est beaucoup plus simple.
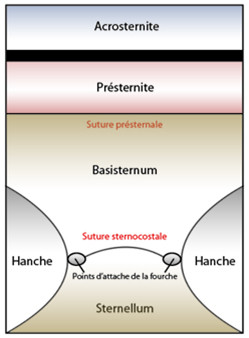
Associé à l’acrotergite, il y a l’acrosternite, celui-ci reste isolé du sternite vrai, cet acrosternite porte le nom d’intersternite ou spinasternite (du fait qu’il y a une crête interne) [Roth, 1980].
Les sternites vrais portent une formation interne, la furca. Cette furca, ou fourche, possède deux points d’attache, points d’attache reliés par une crête dont la trace externe est la suture sternocosale. Le sternum est ainsi séparé en deux parties, le basisternum qui est antérieur et le sternellum (ou furcasternum) qui est postérieur [Roth, 1980].
On note également une suture présternale qui isole le presternum en avant du basisternum.
LES PLEURES
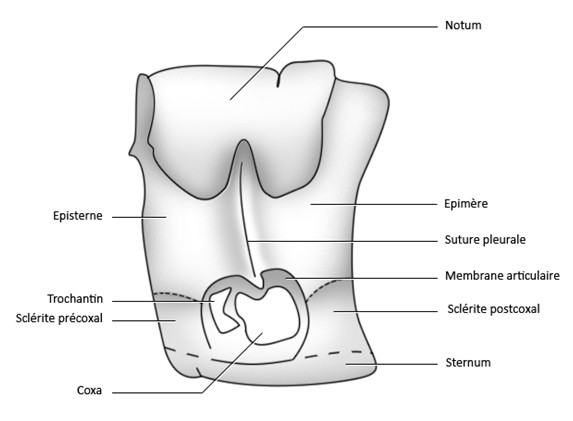
Les pleures sont dues à l’étalement d’articles coxaux sur les deux côtés du thorax, il est couramment admis qu’il s’agit d’un seul article, le subcoxa (expansion du coxopodite) qui s’étale en trois sclérites, les catapleurites, les trochantins et les anopleurites [Roth, 1980].
Ces trois sclérites forment une partie pleurale qu’on nomme la podopleure. A côté de cette partie, il y en a une seconde issue de la métamérisation originelle, la troncopleure (qui porte, les sclérites auxiliaires comme les sclérites précoxaux et postcoxaux, les stigmates et leurs muscles).
Il existe deux schémas types :
- Chez les aptérygotes, les pleures sont formés de trois sclérites, le trochantin, les catapleurites et les anopleurites. Ces derniers étant disposés en anneau autour de la hanche.
- Chez les ptérygotes il existe une suture verticale qui coupe la podopleure en deux parties, l’épisterne en avant et l’épimère en arrière. La suture est qualifiée de pleurale.
De ces schémas types, peuvent dévier quelques autres structures. Ainsi on peut trouver une suture horizontale qui coupera également la podopleure en quatre parties, le supra épisterne, l’infra épisterne, le supra épimère et l’infra épimère. « supra » qualifiant, bien évidemment, la partie au-dessus de la suture et « infra » la partie sous la suture.
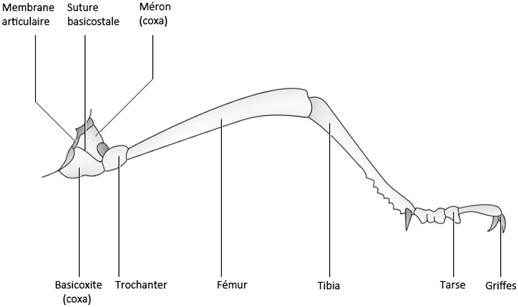
LES PATTES
Les pattes ont une structure commune présentant peu de variation et commencent toutes par une pièce qu’on nomme la hanche ou le coxa. S’en suivent, le trochanter, le fémur, le tibia, le tarse (composé d’un nombre variable de segments) et les griffes [Roth, 1980].
Très souvent ces articles sont associés entre eux par des membranes, n’empêchant pas l’apparition éventuelle d’une articulation faite d’une ou de deux pièces.
La hanche présente à sa base une suture, la suture basicostale qui isole le basicoxite. Cette suture longe la suture pleurale et isole une pièce, le meron.
Le trochanter est une pièce qu’on pourrait croire anecdotique, cependant elle contient des muscles utiles pour rétracter le fémur.
La succession des autres pièces des pattes est toujours identique, mais selon l’ordre ces segments sont plus ou moins modifiés. Ainsi on note chez les mantes et mantispes une transformation des pattes antérieures en pattes ravisseuses, alors que chez les orthoptères, il y a une élongation du fémur et du tibia des pattes postérieures permettant le saut.
LES AILES
À l’heure actuelle, les entomologistes admettent que les ailes sont des expansions notales qui se seraient développées afin de permettre le vol (apparition d’une musculature propre, réduction de l’épaisseur pour donner des membranes, apparition de nervures, etc.)
Les pleures ont un rôle de soutien de ces évaginations.
Le développement des ailes dépendra de l’ordre et surtout du mode de développement de l’insecte.
- Chez les holométaboles, les ailes n’apparaissent qu’après la nymphose.
- Chez les hémimétaboles les ailes se développent dans les bourgeons allaires
Le développement des ailes apparait donc plus ou moins tard selon le mode de développement, cependant il reste identique dans son fond. Lors du développement, deux couches de cellules se superposent au niveau de ce que nous appellerons par souci de compréhension, les bourgeons allaires. Les cellules qui donneront respectivement la partie supérieure et inférieure de l’aile. Ces deux couches fusionneront au niveau de leur lame basale pour donner une membrane homogène, excepté au niveau de certaines lignes, les nervures [Roth, 1980].
Les nervures jouent un rôle de structure pour l’aile, un peu comme le squelette des oiseaux ou des chauves-souris. De plus, en jouant avec un mécanisme de turgescence, elles participent grandement à l’étirement des ailes, lui-même permettant le vol. Le principe est assez simple, lorsque l’animal a besoin de ces ailes, l’hémolymphe est propulsée dans les nervures, les rendant plus épaisses, ce mécanisme s’appelle la turgescence. Lorsque les nervures sont dans cet état, les membranes associées se dressent afin d’augmenter la surface portante de l’insecte sans augmenter son volume.
Il est important de préciser que les nervures contiennent également des trachées et des nerfs et qu’elles sont un critère d’identification très important chez les ptérygotes.
LA NERVATION
Les nervures longitudinales [Jeannel, 1946].
Il est possible de distinguer plusieurs nervures principales pouvant se diviser en plusieurs (souvent deux ou quatre) rameaux, la nervure médiane peut se séparer en 4 branches (M1, M2, M3 et M4), 3, (M1, M3 et M4) ou 2 (M.ant et M.post).
Le bord antérieur de l’aile est bordé par une nervure, la nervure costale ou nervure C. toujours unique, elle peut englober l’aile, elle est alors qualifiée d’enveloppante, ou s’arrêter au niveau de la nervure médiane. Derrière elle, se trouve la nervure sous-costale (ou Sc) pouvant se diviser en deux rameaux.
Plus postérieurement il y a la nervure radiale ou nervure R1, encore une fois unique. Sous elle se situe le secteur radial regroupant jusqu’à 4 nervures R2, R3, R4 et R5, souvent il n’y en a que deux, les branches R2+3 (ou SR1) et R4+5 (ou SR2).
Viennent ensuite les nervures radiales, les nervures cubitales (Cu1 et Cu2) puis les nervures annales (en nombre très variable selon les ordres).
Chez les insectes primitifs, des nervures longitudinales surnuméraires peuvent être présentes
Les nervures transversales [Jeannel, 1946].
Pour bien soutenir l’aile, d’autres nervures sont essentielles, les nervures transversales. La nervure humérale relie les nervures costales et sous-costales. Il y a également des nervures médianes-radiales et radiales-cubitales.
Les nervures peuvent former des espaces clôt, ces espaces sont appelés des cellules ou des aréoles.
Bien entendu la nervation est très différente selon l’ordre d’insecte auquel on s’intéresse.
L’ensemble des nervures est regroupé en 2 zones, le remigium en avant et le vannus en arrière. Chez les néoptères il y a, en arrière, apparition d’une zone lobée séparée du vannus par le pli jugal ou plica jugalis, le champ jugal, encore nommé jugum ou neala.
Les nervures sont articulées avec des sclérites spéciaux qui se trouvent à la base de l’aile. À la base de la nervure costale, il y a un sclérite huméral. trois autres sclérites axillaires sont associés aux autres nervures (Sc à x), soit directement, soit par l'intermédiaire de deux plaques médianes.

Le premier sclérite axillaire s'appuie sur le processus notal antérieur, il s'oppose, par son autre face, au deuxième sclérite axillaire et pousse un prolongement vers la nervure sous-costale sans s’y souder.
La forme du deuxième sclérite axillaire, il est situé entre le premier sclérite axillaire et la première plaque, il est soudé à la nervure radiale R1 et forme le pivot de l’aile.
Le troisième a également une forme variable, il est en relation avec le processus notal postérieur, le deuxième sclérite axillaire et la première plaque. Il commande tout particulièrement les nervures du vannus, c'est sur lui que s'attachent les muscles fléchisseurs de l'aile.
Il existe parfois un quatrième sclérite axillaire, il s'interpose alors entre le troisième et le processus notal postérieur.
Pour conclure sur la structure des ailes, il y a vers la base antérieure de l’aile un petit lobe, nommé tegula, chez certaines familles il peut être très développé et recouvrir la base de l’aile. Parfois, il se développe aussi un lobe postérieur, il est alors cerclé d'une sorte de ligament, la corde axillaire.

Couplage des ailes
La majorité des insectes tétraptères possèdent un système d’accroche entre les ailes antérieures et postérieures d’un même côté. Ce couplage permet une synchronisation des mouvements pendant le vol. Plusieurs mécanismes existent [Aguilar, 2004].
Chez les Lépidoptères, il y en a, par exemple, trois. Le couplage de type jugate où le jugum de l’aile antérieure passe sous l’aile postérieure de sorte que les ailes s’encastrent parfaitement.

Figure 39 : (1) couplage des ailes de type jugate chez Epimartyria auricrinella © microleps.org (2) Couplage de type Frenate chez Oiketicus sp. © wikipedia.org (3) Couplage de type Frenate chez une femelle de Tineidae © microleps.org (4) Couplage des ailes d’un hyménoptère assurée par une rangée de crochets (hamuli) et une gouttière
Le second couplage est le couplage frenate qui existe chez une grande majorité des papillons.
L’accrochage est réalisé via deux structures, un frein (ou frenelum) constitué d’une (chez les mâles) ou plusieurs soies (chez les femelles) et le rétinacle constitué d’un crochet (chez les mâles) ou d’une rangée de soies (chez les femelles) [Aguilar, 2004 ; Ramel, 2014].
Le dernier couplage est une régression du second, il s’agit du couplage amplexiforme qui représente une adhérence entre les deux ailes rendue possible grâce à une dilatation de la région costale de l’aile postérieure [Aguilar, 2004].
Chez les trichoptères il existe des couplages analogues. Chez les Psocoptères, le couplage est assez complexe et sera décrit dans un chapitre dédié.
Chez les autres insectes le couplage est assuré par des épaississements des gouttières ou des crochets.
2.3.3. L'abdomen
MORPHOLOGIE DES SEGMENTS
Les segments abdominaux sont des segments secondaires typiques (décrit précédemment). Cependant, il y a des différences morphologiques en fonction de l’ordre. Embryologiquement, il y a douze segments abdominaux, chez les insectes primitifs, dix ou onze restent visibles, chez les plus évolués il y a habituellement neuf segments voire cinq ou six chez les coléoptères. Il semble donc intéressant de noter qu’il y aurait une réduction du nombre de segments en fonction de l’évolution de l’insecte [Roth, 1980]. D’autres auteurs suggèrent que les segments s’invaginent à l’intérieur de l’abdomen ou participent à la confection des pièces génitales [Aguilar, 2004].
En termes de morphologie. Chez les insectes primitifs, la métamérisation est respectée avec un tergum, un sternum et des pleures plus ou moins sclérifiés, cependant chez les insectes évolués, le sternum peut se souder avec les pleures pour donner une plaque sternale, à l’inverse il se peut que ce soit le tergum qui fusionne avec les pleures. Dans l’un des deux cas, les stigmates associés à l’abdomen vont se trouver sur une membrane, sur un latérotergite ou un latérosternite [Roth, 1980]. Les segments les plus modifiés sont ceux portant les pièces génitales (ou génitalia), généralement il s’agit du neuvième segment chez le mâle, du septième, du huitième ou du neuvième pour la femelle.
En ce qui concerne les segments postérieurs :
- Le dixième segment, qui absorbe souvent le onzième, peut porter des sortes d’appendices comme les cerques ou les socii des lépidoptères. Cependant il ne faut pas les assimiler aux appendices articulés.
- Le onzième segment est atrophié chez la plupart des holométaboles, lorsqu’il existe, il porte l’épiprocte et les paraproctes.
LES GENITALIA
Il est essentiel de s’intéresser aux genitalia, car il se trouve qu’elles sont de plus en plus utilisées en systématique pour reconnaître l’espèce (chez les odonates par exemple). Il est donc très important de bien les connaître pour savoir les disséquer et les étudier sans erreurs.
- Les pièces génitales externes des mâles sont, le plus souvent, un assemblage de plusieurs éléments :
-
- Des pièces servant à assurer l’accolement des organes génitaux (claspers, harpogones, paramères, organes périphalliques, etc.) parfois ce sont les cerques qui jouent ce rôle. Les harpogones sont des organes pairs et mobiles, ils sont portés par le neuvième segment abdominal et sont parfois en relation avec d’autres lobes, non mobiles, issus du tergum ou du sternum (paramères, organes phalliques, etc.).
-
- Presque toujours, il y a un pénis (pouvant être afonctionnel) qui est en général placé dans la membrane articulaire située entre les neuvièmes et dixièmes segments.
- Presque toujours, il y a un pénis (pouvant être afonctionnel) qui est en général placé dans la membrane articulaire située entre les neuvièmes et dixièmes segments.
- Chez les femelles, la différenciation est moins flagrante, la seule adaptation notable est la formation d’ovipositeurs, chez
certains groupes taxonomiques, à partir d’éléments du huitième et du neuvième segment. Lorsque cet élément n’existe pas, les œufs sont souvent collés à différents substrats.
Aucun schéma type ne peut être donné, car les pièces génitales changent beaucoup entre les espèces.
AUTRES APPENDICES
L’extrémité de l’abdomen peut porter d’autres appendices. Les cerques, les urogomphes, les cornicules, les oviscaptes, un aiguillon ou une pince ou forceps